CONTOH SOAL DISERTAI PEMBAHASAN MENGENAI PENGHITUNGAN JUMLAH KALOR
Bismillahirrahmanirrahiim
Selamat datang di situs IPA MTs
be smart with science
Materi kalor merupakan salah satu materi IPA Terpadu di kelas 7. Salah satu pembahasannya adalah menghitung jumlah kalor pada zat yang dipanaskan, seperti es batu yang diletakkan di dalam gelas sehingg es tersebut mencair seluruhnya atau air yang dimasak sampai berubah menjadi uap.
Artikel ini akan menampilkan penjelasan singkat mengenai kalor dan beberapa soal mengenai kalor disertai jawabannya agar kamu dapat memahami cara menyelesaikan soal yang berkaitan dengan penghitungan kalor. Mudah-mudahan dapat bermanfaat dalam menambah pemahaman tentang kalor dan cara menghitung jumlah kalor. Artikel ini dapat diakses di ipamts.com.
Materi Singkat Tentang Kalor
Kalor disebut juga panas. Kalor termasuk besaran turunan dan besaran skalar. Satuan kalor adalah Joule atau kalori. 1 kalori = 4,2 Joule. Berikut hal-hal yang berkaitan dengan kalor :
- Kalor dapat merubah suhu zat. Jumlah kalor yang dibutuhkan untuk menaikkan suhu zat dihitung dengan rumus Q = m . c . 𝚫t dimana m adalah massa zat dengan satuan kilogram (kg). c adalah kalor jenis zat dengan satuan J/KgºC. 𝚫t adalah kenaikan suhu (selisih suhu akhir zat dengan suhu awal zat) dengan satuan ºC. Rumus 𝚫t = t₂-t₁.
- Kalor dapat merubah wujud zat. Ketika zat diberi kalor maka zat tersebut dapat melebur dan menguap. Jumlah kalor yang diperlukan untuk meleburkan zat dihitung dengan rumus Q=m.L, dimana Q adalah jumlah kalor dengan satuan Joule (J), m adalah massa zat yang diberi kalor dengan satuan Kilogram (Kg) dan L adalah kalor lebur zat dengan satuan J/Kg. Adapun kalor uap dihitung dengan rumus Q=m.U dengan U adalah kalor uap zat dengan satuan J/Kg.
- Bila terjadi pencampuran dua zat yang berbeda suhu maka berlaku rumus azas black dimana jumlah kalor yang dilepas zat bersuhu tinggi sama dengan kalor yang diterima zat yang bersuhu rendah. Rumusnya adalah Qdilepas = Qditerima. m₁.c₁.(t₁-tₐ) = m₂.c₂.(tₐ-t₂)
- Kalor dapat berpindah dengan 3 cara yaitu konduksi, konveksi dan radiasi
Berdasarkan uraian singkat di atas dapat diketahui bahwa terdapat 3 rumus yang digunakan untuk menghitung jumlah kalor yaitu :
- Q = m.c.𝚫t, rumus ini digunakan saat terjadi kenaikan suhu
- Q = m.L, rumus ini digunakan saat zat tersebut melebur
- Q = m.U, rumus ini digunakan saat zat tersebut menguap
Baca juga : Trik mengerjakan soal kesetaraan suhu pada termometer
Contoh Soal dan Pembahasan
1. Berapa jumlah kalor yang dibutuhkan untuk menaikkan suhu 500 gram air dari suhu 20ºC menjadi 50ºC, jika diketahui kalor jenis air adalah 4.200 J/KgºC?
Pembahasan :
Diketahui :
- m = 500 gram = 500/1000 Kg = 0,5 Kg
- cₐ = 4.200 J/KgºC
- 𝚫t = 50ºC - 20ºC = 30ºC
Ditanyakan :
- Q = .... J ?
Jawab :
- Q = m.c.𝚫t
- Q = 0,5 Kg. 4.200 J/KgºC . 30ºC
- Q = 63.000 J
- Q = 6,3 x 10⁴ J
- Q = 63 KJ
2. Sebongkah es dengan massa 150 gram dan suhu -4ºC dipanaskan sehingga melebut menjadi air seluruhnya. Jika kalor jenis es 2100 J/KgºC dan kalor jenis air 4200 J/KgºC serta kalor lebur es 340.000 J/Kg, maka jumlah kalor yang dibutuhkan untuk meleburkan es adalah....
Pembahasan :
Diketahui :
- mₑₛ = 150 gram = 150/1000 Kg = 0,15 Kg
- cₑₛ = 2100 J/KgºC
- cₐ = 4200 J/KgºC
- Lₑₛ = 340.000 J/Kg
- 𝚫t = 0ºC - (-4ºC) = 4ºC. Ingat es melebur seluruhnya pada suhu 0ºC
Ditanyakan :
- Q untuk meleburkan es = ..... J ?
Jawaban :
- Pada pertanyaan di atas, kamu perlu menghitung jumlah kalor untuk menaikkan suhu es dari -4ºC sampai 0ºC dan jumlah kalor untuk meleburkan es seluruhnya kemudian hasilnya dijumlahkan.
- Q = Qmenaikkan suhu es sampai ke titik lebur + Qmeleburkan es
- Q = mₑₛ.cₑₛ.𝚫t + mₑₛ.Lₑₛ
- Q = 0,15 Kg.2100 J/KgºC.4ºC + 0,15 Kg.340.000 J/Kg
- Q = 52.260 J
- Q = 5,26 x 10⁴ J
- Q = 52,26 KJ
3. Kalor sebanyak 84 KJ digunakan untuk memanaskan air 500 gram yang bersuhu 20ºC. Jika kalor jenis air 4200 J/KgºC, maka suhu air setelah dipanaskan adalah....
Pembahasan :
Diketahui :
- Q = 84 KJ = 84.000 J
- m = 500 gram = 500/1000 Kg = 0,5 Kg
- t₁ = 20ºC
- c = 4200 J/KgºC
Ditanyakan :
- Suhu air setelah dipanaskan (t₂) = ....ºC ?
Jawaban :
- Q = m.c.𝚫t = m.c.(t₂-t₁). Karena yang dicari adalah suhu akhir (t₂) maka rumusnya adalah
- t₂-t₁ = Q/m.c
- t₂ = Q/m.c + t₁, setalah itu kamu masukkan nilai dari masing-masing besaran tersebut.
- t₂ = (84.000 J/0,5 Kg.4200 J/KgºC) + 20ºC
- t₂ = 40ºC + 20ºC
- t₂ = 60ºC
4. Sebongkah es mempunyai massa 200 gram dengan suhu -5ºC dipanaskan dengan energi sebesar 50.000 kalori. Diketahui kalor lebur es 80 kal/g, kalor jenis es 0,5 kal/gºC, kalor jenis air 1 kal/gºC dan kalor uap air 540 kal/g. Wujud es pada akhir pemanasan adalah....
- A. sebagian berwujud cair dan sebagian berubah menjadi gas
- B. semua berwujud cair
- C. sebagian berwujud cair, sebagian berwujud padat
- D. semua berwujud padat
Pembahasan :
Diketahui :
- m = 200 g
- t₁ = -5ºC
- Q = 50.000 kalori
- cₑₛ = 0,5 kal/gºC
- cₔ = 1 kal/gºC
- Lₑₛ = 80 kal/g
- Uₔ = 540 kal/g
Ditanyakan :
- Wujud es pada akhir pemanasan ?
Jawab :
Untuk menjawab pertanyaan ini, kamu harus menghitung jumlah kalor untuk menaikkan suhu es ke 0ºC, jumlah kalor untuk meleburkan es, jumlah kalor untuk menaikkan air dari 0ºC sampai 100ºC dan jumlah kalor uap air kemudian membandingkannya dengan jumlah kalor yang tersedia yaitu 50.000 kalori.
a. Jumlah kalor untuk menaikkan suhu es dari -5ºC - 0ºC
- Q = m.cₑₛ.𝚫t
- Q = 200 g.0,5 kal/gºC.(0ºC-(-5ºC))
- Q = 500 kal
b. Jumlah kalor untuk meleburkan es
- Q = m.Lₑₛ
- Q = 200g.80kal/g
- Q = 16.000 kal
c. Jumlah kalor untuk menaikkan suhu air dari 0ºC - 100ºC
- Q = m.cₔ.𝚫t
- Q = 200g.1 kal/gºC.(100ºC-0ºC)
- Q = 20.000 kal
d. Jumlah kalor untuk menguapkan air
- Q = m.Uₔ
- Q = 200g.540 kal/g
- Q = 108.000 kal
Berdasarkan penghitungan tersebut dapat diketahui bahwa untuk menaikkan suhu air sampai 100ºC membutuhkan kalor sebesar 20.000 kalori, sedangkan untuk menguapkan air seluruhnya dibutuhkan kalor sebesar 108.000 kal. Adapun kalor yang tersedia adalah 50.000 kal. Jadi dengan kalor 50.000 kal, dapat menaikkan suhu air sampai titik didih uapnya sehingga menguap sebagian. Wujud bongkahan es tersebut, sebagiannya sudah berwujud cair dan sebagiannya berwujud gas (A)
5. Andi menemukan logam yang bermassa 600 gram. Ketika dipanaskan dari suhu 25ºC hingga 65ºC diperlukan kalor 11,04 KJ. Jenis logam dan kalor jenis yang benar adalah....
- A. timah dengan kalor jenis 130 J/KgºC
- B. perak dengan kalor jenis 230 J/KgºC
- C. tembaga dengan kalor jenis 390 J/KgºC
- D. besi dengan kalor jenis 460 J/KgºC
Pembahasan :
Untuk menjawab pertanyaan tersebut, kamu harus menghitung kalor jenis dari logam yang ditemukan Andi kemudian dicocokan dengan pilihan yang ada. Rumus untuk menghitung kalor jenis adalah c = Q/m.𝚫t
Diketahui :
- m = 600 gram = 0,6 Kg
- 𝚫t = 65ºC - 25ºC = 40ºC
- Q = 11,04 KJ = 11,04 x 1000 J = 11.040 J
Ditanyakan :
- c = .....J/KgºC ?
Jawaban :
- c = Q/m.𝚫t
- c = 11.040 J/0,6 Kg.40ºC
- c = 460 J/KgºC
- Logam dengan kalor jenis 460 J/KgºC adalah besi (D)
6. Perhatikan tabel kalor jenis berikut :
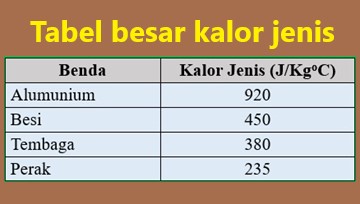 |
| Tabel kalor jenis benda |
Logam X bermassa 4,2 Kg dipanaskan hingga suhunya 140ºC, kemudian dimasukkan ke dalam 9,2 Kg air yang suhunya 30ºC. Setelah beberapa saat terjadi keseimbangan, dimana suhu akhir campuran menjadi 40ºC. Bila kalor jenis air 4200 J/KgºC, maka dapat disimpulkan bahwa jenis logam X adalah....
- A. Alumunium
- B. Besi
- C. Tembaga
- D. Perak
Pembahasan :
Menjawab pertanyaan di atas, gunakan asas Black karena ada dua campuran zat dengan suhu berbeda kemudian hitung kalor jenis logam X berdasarkan rumus asas black tersebut. Benda dengan suhu tinggi ditulis dengan benda 1 dan benda dengan suhu rendah ditulis dengan benda 2
Diketahui :
- m₁ = 4,2 Kg
- t₁ = 140ºC
- m₂ = 9,2 Kg
- t₂ = 30ºC
- tₐ = 40ºC
- c₂ = 4200 J/KgºC
Ditanyakan :
- c₁ = ......J/KgºC ?
Jawaban :
- Qdilepas = Qditerima
- m₁.c₁.(t₁-tₐ) = m₂.c₂.(tₐ-t₂)
- 4,2 Kg.c₁.(140ºC-40ºC) = 9,2 Kg.4200 J/KgºC.(40ºC-30ºC)
- 420.c₁ = 386.400
- c₁ = 386.400/420
- c₁ = 920 J/KgºC (A)
Penutup
Demikian contoh soal beserta pembahasan tentang materi kalor. Bila ada pertanyaan silahkan ajukan di hubungi kami. Silahkan cari artikel lainnya di situs IPA MTs dengan menggunakan fitur pencarian. Jika artikel ini bermanfaat, kami berharap kamu dapat membagikannya kepada teman-temanmu agar mereka dapat memahami persoalan tentang penghitungan jumlah kalor.
